Dienstleistung Swiss Medtech Expo 2023
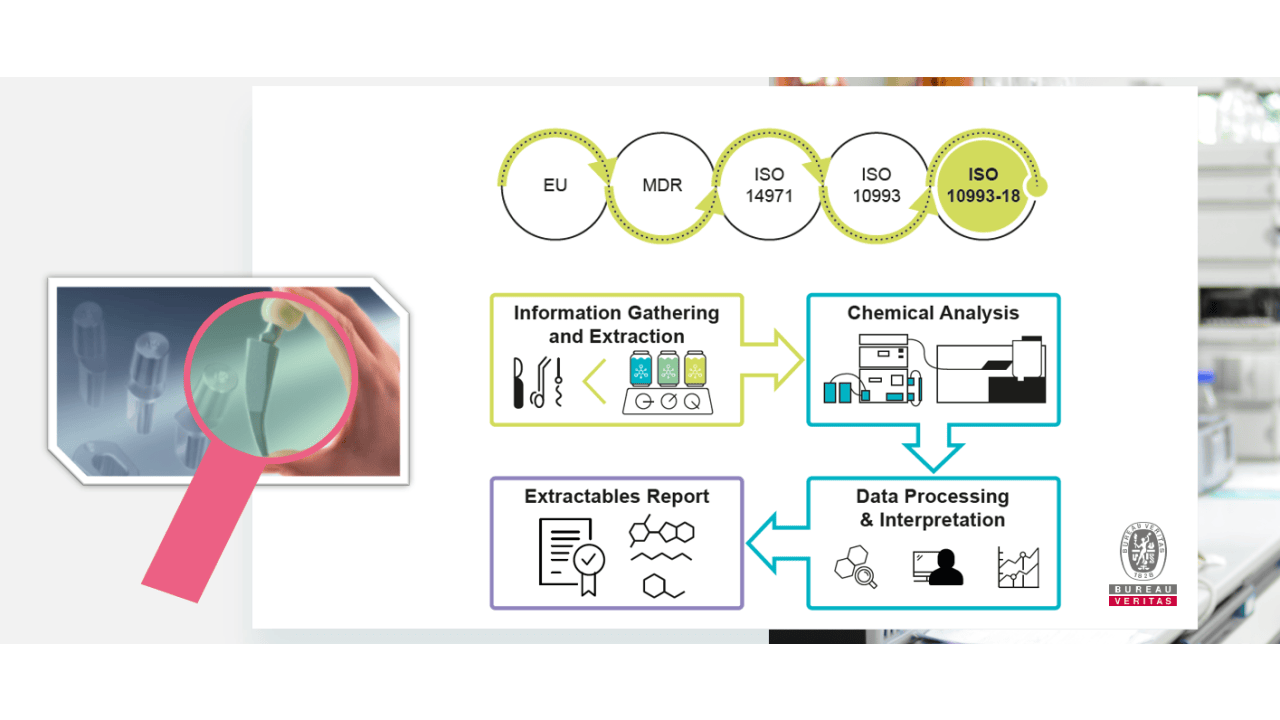
ISO 10993: Biokompatibilität
Die Anforderungen an das Risikomanagement gemäß ISO 14971 für die biologische Beurteilung von Medizinprodukten hat sich grundlegend geändert. Gerne unterstützen wir Sie als Experten der ISO 10993-18: "chemische Charakterisierung" dabei, die neuen Herausforderungen zu bewältigen.