Die neue EU-Medizinprodukteverordnung MDR betrifft alle und es stehen nur noch wenige Monate zur Verfügung, bis wichtige Übergangsfristen zur Zertifizierung der Medizinprodukte für die Hersteller ablaufen. Erfahren Sie mehr über wichtige Neuerungen.
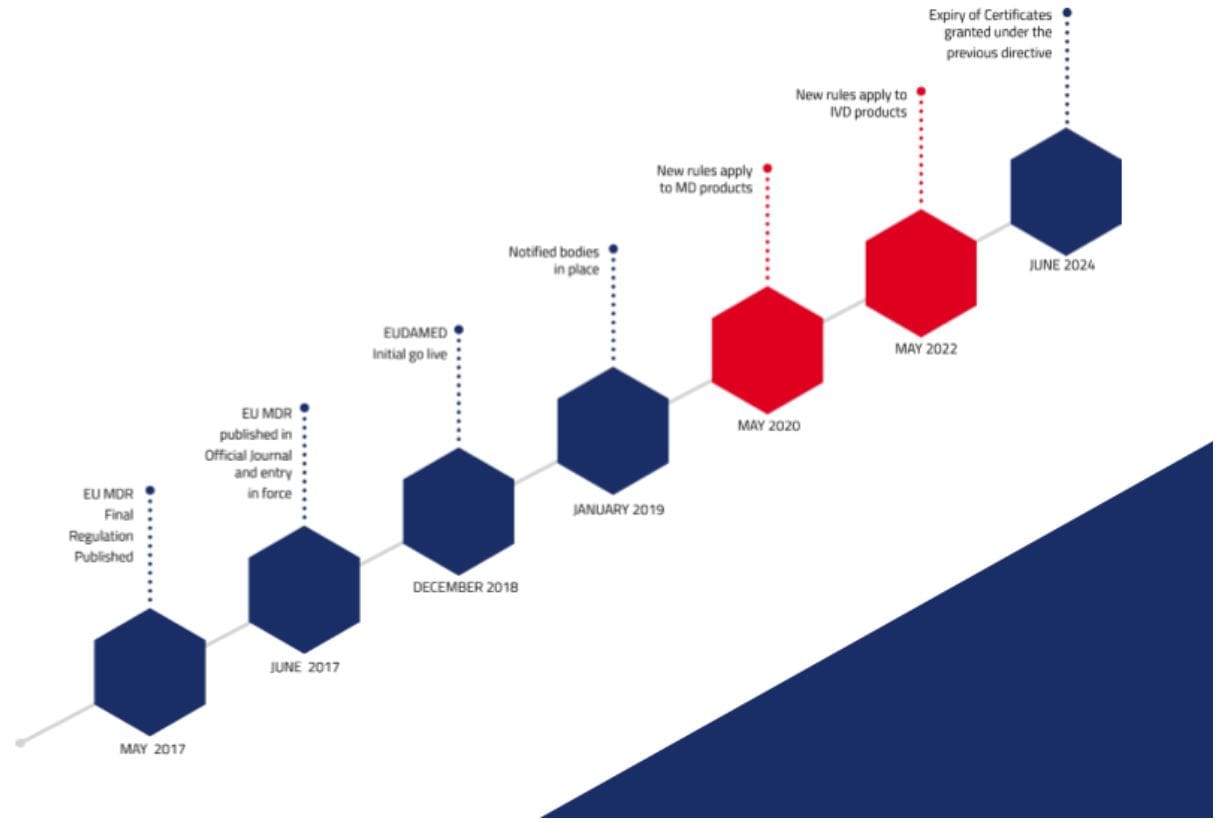
Die neue EU-Medizinprodukteverordnung MDR betrifft alle: Hersteller, Ärzte und Zahnärzte, Zahntechniker, Kliniken, Universitäten und die Patienten. Die MDR ist seit Mitte 2017 in Kraft und hat unmittelbare Wirkung. Im Mai 2020 laufen wichtige Übergangsfristen zur Zertifizierung der Medizinprodukte für die Hersteller ab, doch bislang gibt es europaweit nur zwei nach MDR zugelassene Prüfstellen, wobei eine davon vom Brexit betroffen ist.
Wichtige Neuerungen treten in Kraft
Die Punkte umfassen die Einführung des Konsultationsverfahrens im Zusammenhang mit der klinischen Bewertung für aktive Produkte der Risikoklasse IIb, die dem Körper Arzneimittel zuführen oder ableiten, und Implantate der Klasse III (Art. 55 MDR), die Höherklassifizierung u.a. von Software, stofflichen Medizinprodukten und wiederverwendbaren chirurgisch-invasiven Instrumenten. Höhere Anforderungen erfolgen auch an das QMS und an die technische Produktedokumentation. Weiter sind Post-Market-Daten aus dem nun wichtigeren Post-Market-Surveillance Prozess einzubeziehen, mit denen die klinische Bewertung aktualisiert werden muss. Neue Anforderungen werden an die Etikettierung von Medizinprodukten gestellt, beispielsweise mit Einführung einer eindeutigen Produktidentifizierungsnummer (UDI). Zudem sind die Ansprüche an die Wiederaufbereitung von Einmalprodukten gestiegen.
Erfolgreiche Implementierung
Die epmodex GmbH ist darauf spezialisiert, ihre Kunden bei der Umsetzung der neuen Medizinprodukteverordnung zu unterstützen. Erfahren Sie von Martin Epper, Geschäftsführer der epmodex, wie die epmodex ihre Kunden bei der Umsetzung der neuen Medizinprodukteverordnung erfolgreich unterstützt. Er teilt seine Erfahrung aus ausgewählten Projekten und zeigt Ihnen in diesem Showcase, wie Sie die MDR in einfachen Schritten erfolgreich implementieren und dabei Stolpersteine vermeiden.